Kyntra Bio ogłasza pozytywne dane z badania fazy 1b/2 prowadzonego przez badaczy nad preparatem FG-3246 w połączeniu z Enzalutamidem u pacjentów z przerzutowym, opornym na kastrację rakiem prostaty, które zostaną zaprezentowane na ASCO GU 2026
- Terapia skojarzona FG-3246 i enzalutamidem, u pacjentów z przerzutowym rakiem prostaty opornym na kastrację (mCRPC), wcześniej leczonych inhibitorem szlaku receptora androgenowego (ARPI) i nieleczonych taksanami, w populacji bez selekcji biomarkerów, prowadziła do mediany radiograficznego przeżycia wolnego od progresji (rPFS) wynoszącej 7,0 miesiąca w całej kohorcie badania, przy medianie rPFS 10,1 miesiąca u pacjentów, którzy progresowali po tylko jednym wcześniejszym ARPI
- Wyższe wychwytywanie FG-3180, środka do obrazowania PET skierowanego przeciwko CD46, wykazało tendencję do wyższego prawdopodobieństwa odpowiedzi PSA50, podkreślając jego potencjał w selekcji pacjentów
- Terapia skojarzona miała podobny profil bezpieczeństwa i ekspozycji jak wcześniejsze badanie monoterapii FG-3246 fazy 1
- Wyniki dodatkowo potwierdzają kluczowe elementy projektu badania monoterapii FG-3246 fazy 2, w szczególności włączenie pacjentów, którzy progresowali po tylko jednym wcześniejszym ARPI oraz integrację wyjściowego PET FG-3180 dla wszystkich włączonych pacjentów
- Badanie monoterapii FG-3246 fazy 2 jest na dobrej drodze do przeprowadzenia analizy pośredniej w drugiej połowie 2026 roku
SAN FRANCISCO, 23 lutego 2026 (GLOBE NEWSWIRE) -- Kyntra Bio (Nasdaq: KYNB), wcześniej FibroGen (Nasdaq: FGEN), ogłosiła dziś, że dane dotyczące aktywności przeciwnowotworowej FG-3246 w skojarzeniu z enzalutamidem u pacjentów z przerzutowym rakiem prostaty opornym na kastrację (mCRPC) z badania fazy 1b/2 prowadzonego przez badaczy, zostaną zaprezentowane podczas Sympozjum American Society of Clinical Oncology Genitourinary Cancers (ASCO GU), które odbędzie się w dniach 26-28 lutego 2026 roku w San Francisco, CA.
„Wyniki tego badania fazy 1b/2 prowadzonego przez badaczy pokazują obiecującą wstępną aktywność przeciwnowotworową FG-3246 w skojarzeniu z enzalutamidem u pacjentów z mCRPC. Szczególnie istotne jest 10,1 miesiąca rPFS u pacjentów po tylko jednym wcześniejszym ARPI, co podkreśla potencjał FG-3246 we wcześniejszych liniach terapii” - skomentował dr Rahul Aggarwal, profesor medycyny na Uniwersytecie Kalifornijskim w San Francisco i główny badacz. „Pozytywna tendencja zaobserwowana w związku między wychwytem FG-3180 (PET skierowanym przeciwko CD46) a odpowiedzią PSA50, choć na małej liczbie pacjentów, jest szczególnie intrygująca i jestem podekscytowany możliwością dalszego zbadania użyteczności tego biomarkera w badaniu monoterapii fazy 2.”
„Te dane z badania prowadzonego przez badaczy rozszerzają klinicznie istotne wyniki wcześniej zaobserwowane dla FG-3246,” powiedział Thane Wettig, dyrektor generalny Kyntra Bio. „10,1 miesiąca mediany rPFS u pacjentów progresujących po tylko jednym wcześniejszym ARPI oraz ograniczenie działań niepożądanych związanych z neutropenią dzięki profilaktyce G-CSF są szczególnie obiecujące, ponieważ dodatkowo potwierdzają nasz projekt badania monoterapii fazy 2. Z niecierpliwością oczekujemy na udostępnienie analizy pośredniej badania monoterapii fazy 2 w drugiej połowie 2026 roku, jak również na dalszą charakterystykę potencjalnej użyteczności FG-3180 jako biomarkera selekcjonującego pacjentów.”
Prezentacja obejmuje dane od 44 pacjentów bez selekcji biomarkerów z postępującym przerzutowym rakiem prostaty opornym na kastrację, z czego 17 zostało włączonych do części fazy 1b z eskalacją dawki. Kryteria kwalifikacji do badania obejmowały pacjentów, którzy progresowali po co najmniej jednym wcześniejszym ARPI, natomiast pacjenci leczeni wcześniej chemioterapią w ustawieniu oporności na kastrację byli wykluczeni. Ponad 60% pacjentów progresowało po dwóch lub więcej wcześniejszych ARPI, w tym po enzalutamidzie. Głównym punktem końcowym fazy eskalacji była ocena toksyczności ograniczającej dawkę (DLT) oraz określenie maksymalnej tolerowanej dawki i zalecanej dawki dla fazy 2 badania – określonej na poziomie 2,1 mg/kg FG-3246 i 160 mg/dzień enzalutamidu. Głównym punktem końcowym fazy 2 było złożone tempo odpowiedzi (odpowiedź PSA50 i/lub odpowiedź obiektywna zgodnie z RECIST v1.1). Punktami końcowymi drugorzędowymi były: wskaźnik odpowiedzi PSA50, wskaźnik odpowiedzi obiektywnej, radiograficzne przeżycie wolne od progresji (rPFS), całkowite przeżycie oraz działania niepożądane związane z leczeniem (TRAEs).
FG-3246 w połączeniu z enzalutamidem wykazał aktywność przeciwnowotworową ze złożoną częstością odpowiedzi wynoszącą 21% w całej kohorcie oraz 40% u pacjentów, którzy progresowali po tylko jednym wcześniejszym ARPI. Mediana rPFS wyniosła 7,0 miesiąca w całej kohorcie. Co istotne, mediana rPFS 10,1 miesiąca została zaobserwowana u pacjentów progresujących po tylko jednym wcześniejszym ARPI, a wynik ten był spójny dla różnych stosowanych ARPI. Ponadto, wyższy wychwyt FG-3180 wykazał tendencję do wyższego prawdopodobieństwa odpowiedzi PSA50 (p=0,053), co podkreśla potencjał FG-3180 jako biomarkera selekcji pacjentów.
Terapia skojarzona FG-3246 i enzalutamidem wykazała podobny profil bezpieczeństwa jak zaobserwowano w poprzednim badaniu monoterapii FG-3246 fazy 1. Ryzyko neutropenii zostało skutecznie zminimalizowane dzięki zastosowaniu profilaktyki G-CSF. Najczęstsze działania niepożądane związane z leczeniem (TRAEs) w terapii skojarzonej obejmowały zmęczenie, neuropatię obwodową, anoreksję i zaburzenia smaku. Suma toksyczności, w tym neuropatia obwodowa, doprowadziła do przerwania leczenia u części pacjentów.
Prezentacja posterowa, zatytułowana „Badanie fazy 1b/2 FOR46 (FG-3246) w połączeniu z enzalutamidem (enza) u pacjentów z przerzutowym rakiem prostaty opornym na kastrację (mCRPC)”, zaplanowana jest na sesję posterową, która odbędzie się 26 lutego 2026 roku w godz. 11:30-12:45 czasu PT.
FG-3246 jest obecnie oceniany w badaniu monoterapii fazy 2, a dane pośrednie są spodziewane w drugiej połowie 2026 roku. Badanie obejmuje również leczenie FG-3180, środkiem do obrazowania PET skierowanym przeciwko CD46, który mierzy poziomy ekspresji zmian CD46-dodatnich. Umożliwi to dalszą ocenę korelacji między ekspresją CD46 a odpowiedzią na FG-3246 oraz potencjałem FG-3180 jako biomarkera wspomagającego selekcję pacjentów w przyszłych badaniach FG-3246.
O FG-3246 i FG-3180
FG-3246 (FOR46) to potencjalny pierwszy w swojej klasie w pełni ludzki koniugat przeciwciało-lek (ADC), licencjonowany wyłącznie od Fortis Therapeutics, rozwijany przez Kyntra Bio do leczenia przerzutowego raka prostaty opornego na kastrację oraz potencjalnie innych typów nowotworów. FG-3246 wiąże się z epitopem CD46, docelowego receptora komórkowego, który indukuje internalizację po związaniu przeciwciała, jest obecny na wysokim poziomie w raku prostaty i innych nowotworach oraz wykazuje bardzo ograniczoną ekspresję w większości zdrowych tkanek. FG-3246 składa się z przeciwciała anty-CD46, YS5, połączonego z czynnikiem przeciwdziałającym mitozie, MMAE, będącym klinicznie i komercyjnie zweryfikowanym ładunkiem ADC. FG-3246 wykazał aktywność przeciwnowotworową zarówno w badaniach przedklinicznych, jak i klinicznych. FG-3180 jest diagnostycznym środkiem do obrazowania PET, wykorzystującym to samo przeciwciało skierowane przeciwko CD46 wraz z
O badaniu fazy 1b/2 FG-3246 w połączeniu z enzalutamidem
To badanie fazy 1b/2 prowadzone przez badaczy jest realizowane na Uniwersytecie Kalifornijskim w San Francisco, aby ocenić FG-3246 (FOR46) w połączeniu z enzalutamidem u pacjentów z przerzutowym rakiem prostaty opornym na kastrację (mCRPC) po wcześniejszej progresji po co najmniej jednym inhibitorze szlaku receptora androgenowego. Głównym celem fazy 1b badania jest określenie maksymalnej tolerowanej dawki (MTD) i zalecanej dawki fazy 2 FG-3246 w połączeniu z enzalutamidem u pacjentów z mCRPC. Cele fazy 2 badania to określenie złożonego wskaźnika odpowiedzi (CRR), odsetka uczestników z co najmniej 50% zmianą w swoistym antygenie sterczowym (PSA50), wskaźnika odpowiedzi obiektywnej (ORR), mediany czasu trwania odpowiedzi, mediany radiograficznego przeżycia wolnego od progresji (rPFS) oraz mediany całkowitego przeżycia (OS) u pacjentów leczonych FG-3246 w połączeniu z enzalutamidem.
O Kyntra Bio
Kyntra Bio to firma biofarmaceutyczna koncentrująca się na rozwoju nowych terapii onkologicznych i w chorobach rzadkich. Roxadustat (爱瑞卓
Zastrzeżenie: Treść tego artykułu odzwierciedla wyłącznie opinię autora i nie reprezentuje platformy w żadnym charakterze. Niniejszy artykuł nie ma służyć jako punkt odniesienia przy podejmowaniu decyzji inwestycyjnych.
Może Ci się również spodobać
Sprzedaż samochodów w Europie spada w styczniu, gwałtowny spadek samochodów benzynowych
Badanie pokazuje, że amerykańscy inwestorzy detaliczni napędzają wzrost obrotu lewarowanymi ETF
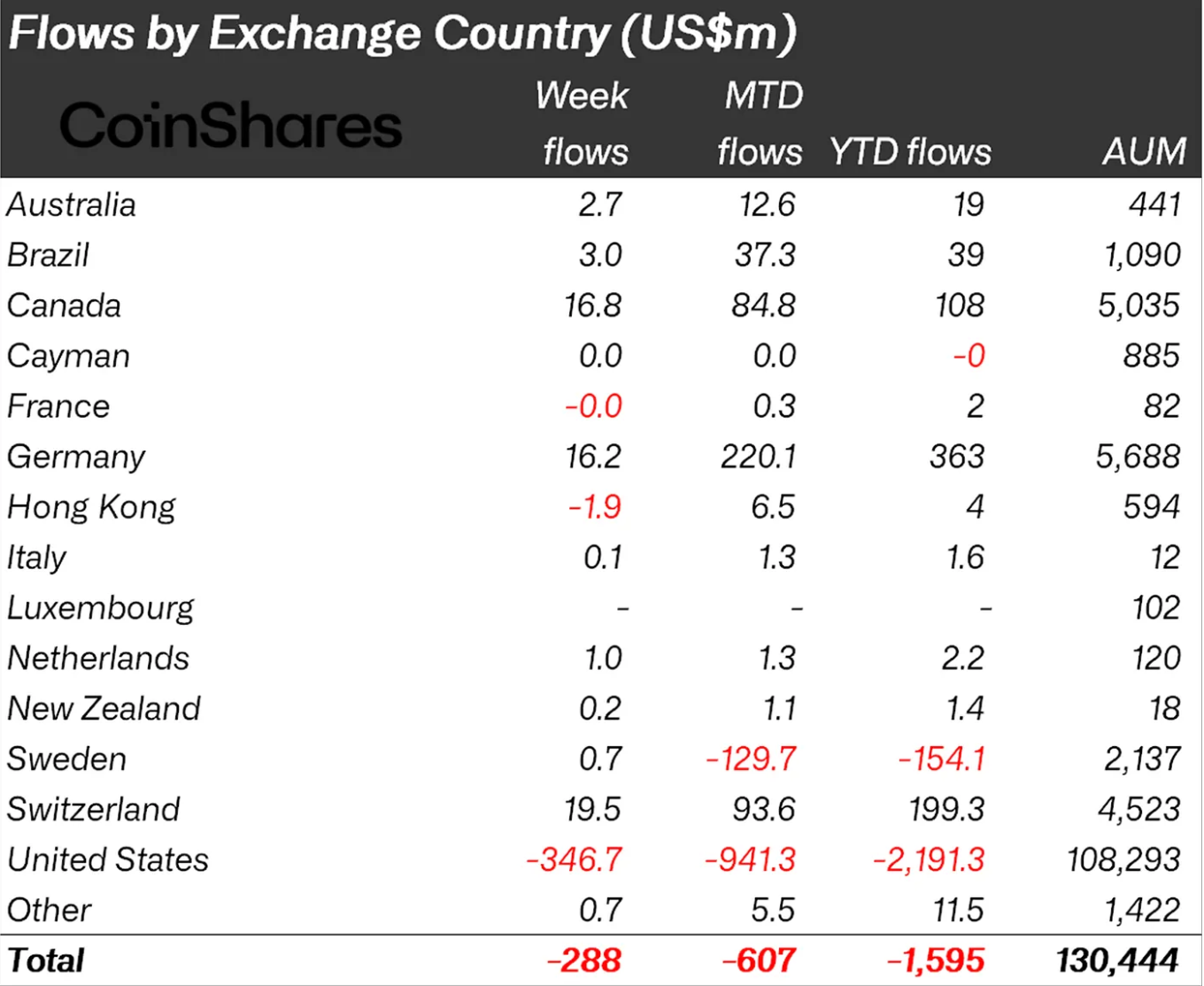
XRP przyciąga napływy, podczas gdy fundusze kryptowalut tracą 288 milionów dolarów
Popularne
WięcejPrognoza wyników finansowych Nvidia za IV kwartał roku fiskalnego 2026: czy wskazówki dotyczące wyników zostaną przebite dzięki wydatkom hiperskalowych klientów na AI na poziomie 600 miliardów dolarów i czy wyniki mogą dalej rosnąć?
Sprzedaż samochodów w Europie spada w styczniu, gwałtowny spadek samochodów benzynowych

