Fulcrum Therapeutics ogłasza pozytywne wyniki po 12 tygodniach z kohorty dawki 20 mg w badaniu fazy 1b PIONEER leku Pociredir u pacjentów z anemią sierpowatą
― Średni bezwzględny poziom hemoglobiny płodowej (HbF) wzrósł o 12,2% (z 7,1% do 19,3%) w 12. tygodniu (n=12), co stanowi szybka, znaczącą i klinicznie istotną odpowiedź, wraz z postępem w kierunku indukcji HbF w całej populacji komórek, ponieważ liczba komórek F wzrosła z 31% do 63% ―
― 7 z 12 pacjentów (58%) osiągnęło bezwzględny poziom HbF ≥20%; wszyscy pacjenci osiągnęli co najmniej 6,5% bezwzględny wzrost HbF ―
― Poprawa markerów hemolizy, poprawiona erytropoeza oraz wzrost całkowitej hemoglobiny o ponad 1 g/dL ―
― 7 z 12 pacjentów (58%) zgłosiło brak epizodów VOC podczas okresu leczenia ―
― Pociredir był ogólnie dobrze tolerowany, bez poważnych działań niepożądanych związanych z leczeniem (SAEs) ―
― Fulcrum planuje rozpoczęcie potencjalnego badania rejestracyjnego w drugiej połowie 2026 roku ―
― Telekonferencja i webcast zaplanowane na dziś na godzinę 14:00 czasu polskiego ―
CAMBRIDGE, Massachusetts, 24 lutego 2026 (GLOBE NEWSWIRE) -- Fulcrum Therapeutics, Inc.
„Dane z 12 tygodni dla pełnej kohorty 20 mg wykazały silną i szybką indukcję HbF oraz postęp w kierunku rozkładu HbF na całą populację komórek, czemu towarzyszyło zmniejszenie markerów hemolizy oraz poprawa anemii,” powiedział Alex C. Sapir, prezes i dyrektor generalny Fulcrum. „Co ważne, osiągnięte poziomy HbF są zgodne z poziomami historycznie powiązanymi ze zmniejszeniem zjawiska sierpowacenia i hemolizy w anemii sierpowatokrwinkowej. Te obiecujące wyniki w ciężkiej populacji pacjentów wzmacniają nasze przekonanie, gdy przygotowujemy się do rozmów z organami regulacyjnymi na temat projektu kolejnego badania.”
„Skala indukcji HbF zaobserwowana przy dawce 20 mg, wraz z równoczesnym wzrostem liczby komórek F i towarzyszącym zmniejszeniem markerów hemolizy oraz poprawą anemii, jest zgodna z tym, czego oczekiwalibyśmy od terapii mogącej zmienić podstawową patofizjologię anemii sierpowatokrwinkowej,” powiedział dr Martin Steinberg, profesor medycyny, pediatrii, patologii i medycyny laboratoryjnej w Boston University Chobanian & Avedisian School of Medicine. „Osiągnięcie poziomów HbF w tym zakresie stanowi ważny krok w kierunku zrozumienia potencjału pociredir w poprawie wyników klinicznych u pacjentów z SCD.”
Projekt badania i podsumowanie danych
PIONEER to otwarte badanie kliniczne fazy 1b z eskalacją dawki, oceniające bezpieczeństwo i skuteczność pociredir, doustnego induktora HbF podawanego raz dziennie, u dorosłych pacjentów z ciężką SCD. Kohorta 20 mg obejmowała dorosłych z ciężką SCD. Na dzień odcięcia danych 23 grudnia 2025, wszyscy 12 kwalifikujących się pacjentów z kohorty 20 mg ukończyło 12-tygodniowy okres leczenia i zostali włączeni do zbioru analizy farmakodynamicznej (PD). Jeden pacjent przerwał leczenie w dniu 1 z powodu niezwiązanego poważnego zdarzenia niepożądanego stopnia 5 i został wyłączony z analizy PD, ale jest uwzględniony w zbiorze analizy bezpieczeństwa. Pięciu pacjentów pozostawało w 4-tygodniowym okresie obserwacji na dzień odcięcia danych. Fulcrum planuje zaprezentować dodatkowe dane z kohorty 20 mg, w tym z 4-tygodniowego okresu obserwacji, podczas przyszłej konferencji medycznej.
Dane z badania PIONEER – kohorta 20 mg
Wyniki 12-tygodniowego okresu leczenia w kohorcie 20 mg badania fazy 1b PIONEER (n=12) przedstawiają się następująco:
- Średni bezwzględny poziom HbF wzrósł o 12,2% po 12 tygodniach leczenia pociredir (w porównaniu do 8,6% w 12. tygodniu w kohorcie 12 mg), rosnąc z poziomu wyjściowego 7,1% do 19,3%. Siedmiu z 12 pacjentów (58%) osiągnęło bezwzględny poziom HbF ≥20% w 12. tygodniu, a wszyscy pacjenci wykazali klinicznie istotny wzrost HbF. Poziomy HbF na poziomie 20% są związane z ~90% pacjentów nie doświadczających epizodów VOC w ciągu roku, na podstawie rzeczywistych danych zaprezentowanych przez Fulcrum na 20. Dorocznej Konferencji Sickle Cell & Thalassemia w październiku 2025.
- Odsetek czerwonych krwinek zawierających HbF (komórki F) wzrósł średnio z 31% na początku badania do 63% w 12. tygodniu (n=10), wskazując na postęp w kierunku indukcji HbF w całej populacji komórek (HbF rozłożony na znaczną część czerwonych krwinek (RBC)). Komórki F są bardziej odporne na sierpowacenie i hemolizę dzięki zahamowaniu polimeryzacji hemoglobiny sierpowatej (HbS) przez HbF. Wyższy odsetek komórek F wiąże się z lepszym zdrowiem RBC.
- Średnie zmiany markerów hemolizy i erytropoezy uległy poprawie podczas 12-tygodniowego okresu leczenia:
- Bilirubina pośrednia spadła o 40% (w porównaniu do 37% w 12. tygodniu w kohorcie 12 mg)
- Dehydrogenaza mleczanowa spadła o 34% (w porównaniu do 28% w 12. tygodniu w kohorcie 12 mg)
- Szerokość rozkładu objętości erytrocytów (RDW) spadła o 26% (w porównaniu do 27% w 12. tygodniu w kohorcie 12 mg)
- Liczba retikulocytów spadła o 42% (w porównaniu do 31% w 12. tygodniu w kohorcie 12 mg)
- Średni poziom hemoglobiny wzrósł o 1,1 g/dL w 12. tygodniu (w porównaniu do 0,9 g/dL w 12. tygodniu w kohorcie 12 mg), rosnąc z poziomu wyjściowego 7,3 g/dL do 8,4 g/dL.
- Na podstawie dokumentacji medycznej prowadzonej przez lekarza prowadzącego z okresu 6-12 miesięcy przed włączeniem do badania, w 12-tygodniowym okresie leczenia spodziewano się około 16 epizodów VOC. Podczas 12-tygodniowego okresu leczenia zgłoszono sześć epizodów VOC. Siedmiu z 12 pacjentów (58%) nie doświadczyło epizodów VOC w czasie leczenia.
Aktualizacja bezpieczeństwa pociredir
- Na dzień odcięcia danych 23 grudnia 2025 r. pociredir podano 148 dorosłym, w tym 89 osobom w wielu kohortach dawkowania do 12 tygodni.
- 103 zdrowych ochotników, w tym 44, którzy otrzymywali pociredir przez 10 do 14 dni
- 45 pacjentów z SCD, którzy otrzymywali pociredir przez okres do 12 tygodni
- Profil bezpieczeństwa obserwowany w kohorcie 20 mg na dzień odcięcia danych 23 grudnia 2025 r. pozostał ogólnie zgodny z wcześniej zgłaszanymi danymi dotyczącymi bezpieczeństwa. Pociredir był ogólnie dobrze tolerowany, bez poważnych działań niepożądanych związanych z leczeniem (SAEs) i bez przerwań leczenia z powodu działań niepożądanych związanych z leczeniem na dzień odcięcia danych 23 grudnia 2025 r.
Kolejne kroki
Fulcrum planuje dostarczyć dodatkowe szczegóły dotyczące projektu kolejnego badania w drugim kwartale 2026 roku, po otrzymaniu protokołu ze spotkania End-of-Phase z FDA. Po otrzymaniu opinii od FDA, Fulcrum planuje rozpocząć potencjalne badanie rejestracyjne w drugiej połowie 2026 roku. Fulcrum zamierza także nawiązać współpracę z Europejską Agencją Leków (EMA) w połowie 2026 roku, aby uzyskać wsparcie dotyczące protokołu i opinii na temat projektu kolejnego badania. Ponadto Fulcrum uruchamia ośrodki do otwartego badania przedłużonego dla uczestników badania PIONEER, aby ocenić bezpieczeństwo i trwałość odpowiedzi na pociredir.
Telekonferencja i webcast
Fulcrum Therapeutics, Inc. zorganizuje dziś o godzinie 14:00 czasu polskiego telekonferencję i webcast z udziałem kierownictwa firmy oraz eksperta medycznego, aby omówić dotychczasowe wyniki badania PIONEER fazy 1b. Osoby zainteresowane mogą się zarejestrować, klikając w podany link. Aby zarejestrować się do udziału w telekonferencji, należy skorzystać z linku konferencyjnego. Po rejestracji uczestnicy otrzymają dane do połączenia i unikalny PIN, umożliwiający dostęp do rozmowy. Wydarzenie będzie dostępne w sekcji „Wydarzenia i prezentacje” w dziale Relacji Inwestorskich na stronie internetowej Fulcrum, a nagranie będzie dostępne po zakończeniu wydarzenia.
O Fulcrum Therapeutics
Fulcrum Therapeutics to biofarmaceutyczna firma na etapie klinicznym, koncentrująca się na opracowywaniu małych cząsteczek poprawiających życie pacjentów z rzadkimi chorobami o podłożu genetycznym w obszarach o dużych niezaspokojonych potrzebach medycznych. Wiodącym programem klinicznym Fulcrum jest pociredir, mała cząsteczka zaprojektowana do zwiększania ekspresji HbF w leczeniu SCD. Fulcrum wykorzystuje własną technologię do identyfikacji celów molekularnych wpływających na ekspresję genów, aby leczyć znaną przyczynę błędnej ekspresji genów.
O pociredir
Pociredir to eksperymentalny, doustny inhibitor małocząsteczkowy Embryonic Ectoderm Development (EED), odkryty przy użyciu własnej technologii Fulcrum. Hamowanie EED prowadzi do silnej deregulacji kluczowych represorów globiny płodowej, w tym BCL11A, powodując wzrost HbF. Pociredir opracowywany jest w leczeniu SCD. W badaniu klinicznym fazy 1b PIONEER u osób z SCD pociredir wykazał zależny od dawki wzrost HbF, indukcję HbF w całej populacji komórek oraz poprawę markerów hemolizy i anemii. W kohortach 12 mg i 20 mg pociredir był ogólnie dobrze tolerowany przez okres do trzech miesięcy, bez zgłaszanych poważnych działań niepożądanych związanych z leczeniem. Pociredir otrzymał od FDA status Fast Track oraz Orphan Drug Designation do leczenia SCD.
O anemii sierpowatokrwinkowej
SCD to genetyczne zaburzenie czerwonych krwinek spowodowane mutacją w genie HBB. Gen ten koduje białko będące kluczowym składnikiem hemoglobiny, kompleksu białkowego, który odpowiada za transport tlenu w organizmie. Skutkiem mutacji jest mniej wydajny transport tlenu i powstawanie czerwonych krwinek o sierpowatym kształcie. Komórki te są znacznie mniej elastyczne niż zdrowe i mogą blokować naczynia krwionośne lub pękać. Osoby z SCD zazwyczaj cierpią na poważne konsekwencje kliniczne, które mogą obejmować anemię, ból, infekcje, udar, choroby serca, nadciśnienie płucne, niewydolność nerek, choroby wątroby oraz skróconą długość życia.
O PIONEER
PIONEER to otwarte badanie kliniczne fazy 1b z eskalacją dawki, oceniające bezpieczeństwo i skuteczność pociredir, doustnego induktora HbF podawanego raz dziennie, u dorosłych pacjentów z ciężką SCD. Drugorzędowe punkty końcowe obejmują indukcję HbF, hemolizę i anemię. Punkty eksploracyjne obejmują ekspresję genów globinowych, % komórek F oraz częstość występowania VOC. Fulcrum zakończył wcześniej kohortę 1 (6 mg, n=10), kohortę 2 (2 mg, n=2), kohortę 3a (12 mg, n=4) i kohortę 3b (12 mg, n=16). Zaktualizowane wyniki kohorty 4 (20 mg, n=12) są prezentowane dziś. Łącznie zarejestrowano 13 pacjentów, ale jedno przerwanie leczenia nastąpiło z powodu śmierci, którą badacz uznał za niezwiązaną z leczeniem po powikłaniach związanych z VOC zgłoszonych w dniu 1 badania. Dane farmakodynamiczne (PD) dla kohorty 4 obejmują 12 pacjentów. Zbiór analizy bezpieczeństwa dla 20 mg obejmuje wszystkich 13 pacjentów, którzy zostali zarejestrowani.
Zastrzeżenie: Treść tego artykułu odzwierciedla wyłącznie opinię autora i nie reprezentuje platformy w żadnym charakterze. Niniejszy artykuł nie ma służyć jako punkt odniesienia przy podejmowaniu decyzji inwestycyjnych.
Może Ci się również spodobać
Warner Bros. Discovery otrzymało nową ofertę przejęcia od Paramount
Novo planuje obniżyć ceny Ozempic i Wegovy w związku z rosnącą konkurencją
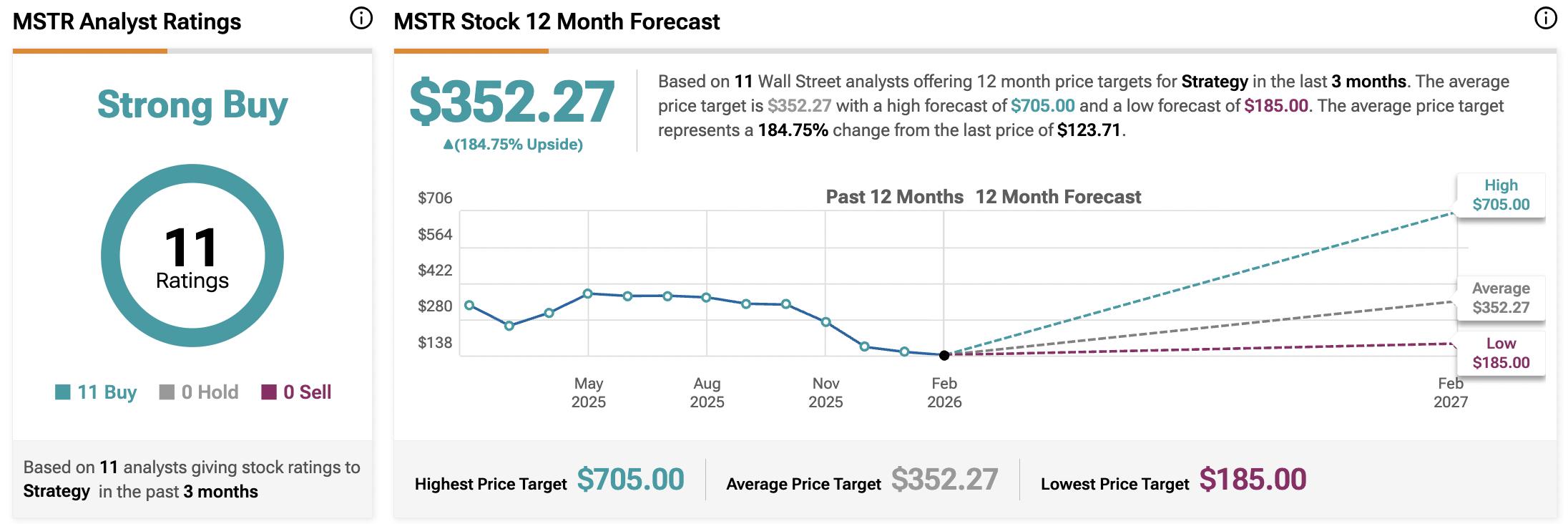
Akcje Strategy uderzają w czerwoną ścianę. 3 powody, dla których akcje Strategy spadają dziś