Europa aprova novo tratamento para asma da GSK administrado duas vezes por ano
A Comissão Europeia aprovou nesta terça-feira o GSK plc’s (NYSE:GSK) Exdensur (depemokimab) para duas indicações, incluindo:
- Como tratamento de manutenção adjuvante para asma grave com inflamação do tipo 2, caracterizada por contagem de eosinófilos no sangue em adultos e adolescentes com 12 anos ou mais que não estão adequadamente controlados, apesar do uso de corticosteroides inalatórios em altas doses mais outro controlador de asma.
- Como terapia adicional com corticosteroides intranasais para pacientes adultos com CRSwNP grave, para quem a terapia com corticosteroides sistêmicos e/ou cirurgia não fornece controle adequado da doença.
A aprovação baseia-se em dados dos ensaios clínicos de fase 3 SWIFT e ANCHOR, que demonstraram eficácia sustentada com um regime de administração semestral para o depemokimab.
Dados do Ensaio
Cada um dos quatro ensaios atingiu seus desfechos primários ou coprimários com resultados estatisticamente significativos e clinicamente relevantes, comparando a adição de depemokimab ao tratamento padrão versus o tratamento padrão isolado.
A asma afeta mais de 42 milhões de pessoas na Europa. Cerca de 5-10% dos pacientes apresentam asma grave, com muitos continuando a sofrer exacerbações e redução da qualidade de vida, apesar do tratamento.
Além disso, pacientes com CRSwNP enfrentam sintomas debilitantes diários, e quase metade permanece sem controle.
Exdensur é uma terapia inovadora que combina alta afinidade de ligação à interleucina-5 (IL-5) e alta potência com uma meia-vida prolongada, permitindo a supressão sustentada da inflamação do tipo 2 que impulsiona a doença, com administração semestral.
Nos ensaios de fase 3 SWIFT, o tratamento com depemokimab resultou em uma redução significativa de 58% e 48% na taxa anualizada de exacerbações de asma (crises de asma) ao longo de 52 semanas para SWIFT-1 e SWIFT-2, respectivamente.
Em um desfecho secundário dos estudos SWIFT-1 e SWIFT-2, os pacientes tratados com depemokimab apresentaram numericamente menos exacerbações que exigiram hospitalização e/ou visitas ao pronto-socorro (1% e 4%) em comparação com o placebo (8% e 10%), respectivamente.
Uma análise agrupada pré-especificada dos dois ensaios mostrou que houve uma redução de 72% na taxa anualizada de exacerbações clinicamente significativas que exigiram hospitalização e/ou visitas ao pronto-socorro ao longo de 52 semanas para depemokimab em comparação com o placebo.
Além disso, nos ensaios de fase 3 ANCHOR, o tratamento com depemokimab resultou em melhora (redução) em relação ao valor basal no escore de pólipo nasal (escala: 0-8) em 52 semanas e na escala de resposta verbal de obstrução nasal nas semanas 49-52.
Contexto
Em dezembro de 2025, a Food and Drug Administration (FDA) dos EUA aprovou o Exdensur como tratamento de manutenção adjuvante da asma grave caracterizada por fenótipo eosinofílico em pacientes com 12 anos ou mais.
Além disso, Exdensur recebeu recentemente aprovação no Reino Unido e no Japão para o tratamento de asma grave e CRSwNP.
Ação de Preço: As ações da GSK subiram 2,65%, a US$ 60,49 durante o pré-mercado, na última verificação de terça-feira, segundo dados do Benzinga Pro.
Foto por JPC_PROD via Shutterstock
Aviso Legal: o conteúdo deste artigo reflete exclusivamente a opinião do autor e não representa a plataforma. Este artigo não deve servir como referência para a tomada de decisões de investimento.
Talvez também goste
Apresentando As (Não) Top 10 Ações da Semana
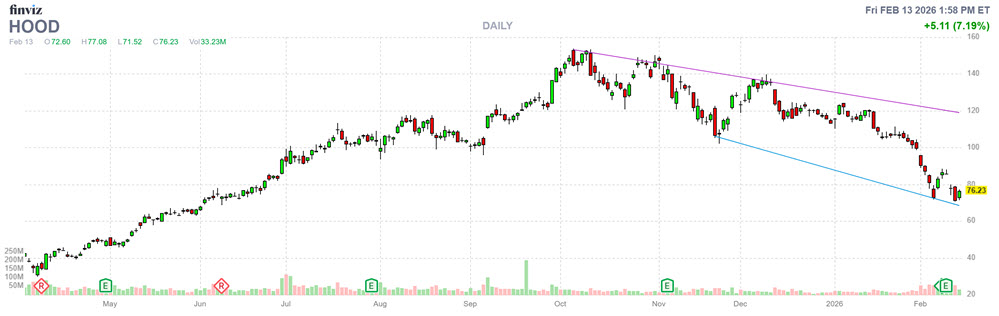
Fabricante britânica de PCs dispara em meio à febre das ‘ações meme’ impulsionada por IA

Ações da Warner Bros sobem nesta terça-feira: O que está acontecendo?
Ações de Precificação e Custos da HRL para Suporte às Margens no Ano Fiscal de 2026