Harrow annonce le lancement des kits PharmaPack à paiement comptant, directement destin�és aux prescripteurs
Programme PharmaPack pour élargir l'accès à des thérapies ophtalmiques de marque, abordables et approuvées par la FDA
NASHVILLE, Tenn., 17 février 2026 (GLOBE NEWSWIRE) -- Harrow (Nasdaq : HROW), un fournisseur de premier plan de solutions de gestion des maladies ophtalmiques en Amérique du Nord, a annoncé aujourd'hui le lancement d'une nouvelle offre Direct-to-Prescriber (DTP) en paiement direct appelée PharmaPack, qui élargit l'engagement de la société à proposer des produits de marque abordables, approuvés par la FDA, en alternative aux formulations magistrales hors AMM.
Les kits PharmaPack élargissent l'accès à des produits ophtalmiques approuvés par la FDA pour les millions d'Américains qui nécessitent chaque année un contrôle des infections et un traitement de la douleur et de l'inflammation associés à la chirurgie de la cataracte. Les kits PharmaPack éliminent également la complexité administrative liée à l'assurance et réduisent les risques réglementaires et médico-légaux associés aux produits magistraux hors AMM. Harrow proposera les kits PharmaPack suivants à des prix abordables et 100 % transparents :
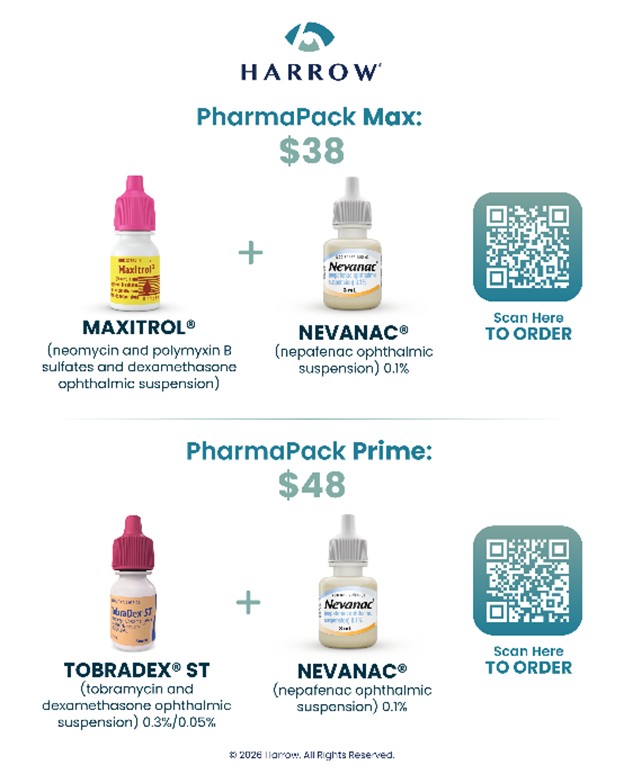
« Le programme PharmaPack de Harrow répond à un défi de longue date en ophtalmologie : fournir aux patients des thérapies approuvées par la FDA qui soient à la fois fiables et abordables », a déclaré le Dr Scott Spector. « La combinaison de produits de marque de confiance, de la transparence des prix et de ces tarifs attractifs en paiement direct est encourageante et facilite une prescription sans complexité, tout en renforçant la confiance lorsqu'on considère des alternatives de marque approuvées par la FDA aux préparations magistrales. Étant donné la force de cette offre et la valeur qu'elle représente, j'ai déjà commandé PharmaPack Prime pour mes patients. »
« L'accès à des thérapies approuvées par la FDA à des prix abordables et transparents est une demande récurrente des optométristes », a déclaré Maria Pribis, OD. « PharmaPack contribue à combler cette lacune en rendant des produits de marque de haute qualité plus accessibles aux soins quotidiens des patients. »
Comment commander :
Les kits PharmaPack seront initialement disponibles en Californie, au Mississippi, en Arkansas, dans le Connecticut et en Alabama, avec des plans d'expansion à l'échelle nationale dans les semaines à venir. Les prescripteurs peuvent accéder aux offres PharmaPack depuis l'écran d'accueil de leur tableau de bord, ou via les liens suivants :
- PharmaPack Max
- PharmaPack Prime
Contactez votre représentant Harrow ou ImprimisRx pour toute question, ou envoyez un e-mail à [email protected].
À propos de NEVANAC
INDICATION ET UTILISATION
La suspension ophtalmique NEVANAC est un promédicament anti-inflammatoire non stéroïdien indiqué pour le traitement de la douleur et de l'inflammation associées à la chirurgie de la cataracte.
CONTRE-INDICATIONS
Hypersensibilité à l’un des ingrédients de la formule ou à d’autres AINS.
AVERTISSEMENTS & PRÉCAUTIONS
- Allongement du temps de saignement : Avec certains anti-inflammatoires non stéroïdiens, y compris NEVANAC ®, il existe un risque potentiel d'allongement du temps de saignement en raison d'une interférence avec l'agrégation thrombocytaire. Il a été signalé que les anti-inflammatoires non stéroïdiens administrés par voie oculaire peuvent augmenter le saignement des tissus oculaires (y compris les hyphémas) lors de la chirurgie oculaire. Il est recommandé d'utiliser la suspension ophtalmique NEVANAC®avec prudence chez les patients présentant des tendances hémorragiques connues ou recevant d'autres médicaments susceptibles de prolonger le temps de saignement.
- Retard de cicatrisation : Les anti-inflammatoires non stéroïdiens topiques (AINS), y compris NEVANAC ®, peuvent ralentir ou retarder la guérison. Les corticostéroïdes topiques sont également connus pour ralentir ou retarder la guérison. L’utilisation concomitante d’AINS topiques et de stéroïdes topiques peut augmenter le risque de problèmes de cicatrisation.
- Effets cornéens : L'utilisation d'AINS topiques peut entraîner une kératite. Chez certains patients sensibles, l'utilisation continue d'AINS topiques peut provoquer une dégradation de l'épithélium, un amincissement cornéen, une érosion cornéenne, un ulcère cornéen ou une perforation cornéenne. Ces événements peuvent mettre en jeu le pronostic visuel. Les patients présentant des signes de dégradation épithéliale cornéenne doivent immédiatement arrêter l'utilisation d'AINS topiques, y compris NEVANAC ®et être étroitement surveillés pour leur santé cornéenne.
L'expérience post-commercialisation avec les AINS topiques suggère que les patients ayant subi des chirurgies oculaires compliquées, une dénervation cornéenne, des défauts épithéliaux cornéens, un diabète sucré, des maladies de la surface oculaire (par ex. syndrome de l'œil sec), une polyarthrite rhumatoïde, ou des chirurgies oculaires répétées sur une courte période peuvent présenter un risque accru d'effets indésirables cornéens potentiellement graves. Les AINS topiques doivent être utilisés avec prudence chez ces patients.
L'expérience post-commercialisation avec les AINS topiques suggère également qu'une utilisation plus de 1 jour avant la chirurgie ou au-delà de 14 jours après la chirurgie peut augmenter le risque et la gravité des effets indésirables cornéens.
- Port de lentilles de contact : NEVANAC ne doit pas être administré lors du port de lentilles de contact.
EFFETS INDÉSIRABLES
Étant donné que les études cliniques sont menées dans des conditions très variées, les taux d'effets indésirables observés dans les études cliniques d'un médicament ne peuvent pas être directement comparés à ceux d'un autre médicament et peuvent ne pas refléter les taux observés en pratique.
Veuillez consulter les informations importantes de sécurité supplémentaires tout au long du document ainsi que la notice complète incluse pour la prescription.
À propos de TOBRADEX
INDICATION ET UTILISATION
TOBRADEX ST (suspension ophtalmique de tobramycine et dexaméthasone) 0,3 %/0,05 % est une combinaison antibiotique topique et corticostéroïde pour les affections inflammatoires oculaires répondant aux stéroïdes et pour lesquelles un corticostéroïde est indiqué et où une infection bactérienne superficielle de l'œil ou un risque d'infection bactérienne oculaire existe.
Informations importantes de sécurité
CONTRE-INDICATIONS :
La plupart des maladies virales de la cornée et de la conjonctive, y compris la kératite herpétique épithéliale (kératite dendritique), la vaccine, la varicelle, ainsi que les infections mycobactériennes de l'œil et les maladies fongiques des structures oculaires. Hypersensibilité à l'un des composants du médicament.
AVERTISSEMENTS & PRÉCAUTIONS :
- Augmentation de la pression intraoculaire (PIO) — Une utilisation prolongée peut entraîner un glaucome avec atteinte du nerf optique et défauts de l'acuité visuelle et du champ visuel. La PIO doit être surveillée.
- Sensibilité aux aminosides — Une sensibilité aux aminosides appliqués localement peut survenir.
- Cataractes — Une formation de cataracte sous-capsulaire postérieure peut survenir.
- Retard de cicatrisation — Peut retarder la guérison et augmenter l'incidence de la formation de bulles filtrantes. Des perforations de la cornée ou de la sclérotique ont été rapportées. Une biomicroscopie à la lampe à fente et une coloration à la fluorescéine doivent être réalisées.
- Infections bactériennes — Peut supprimer la réponse de l'hôte et augmenter les infections oculaires secondaires. En cas d'affections purulentes aiguës, les stéroïdes peuvent masquer ou aggraver une infection existante. Si les signes et symptômes ne s'améliorent pas après 2 jours, le patient doit être réévalué.
- Infections virales — L'utilisation chez des patients ayant des antécédents d'herpès simplex nécessite une grande prudence. L'évolution et la gravité de nombreuses infections virales de l'œil (y compris l'herpès simplex) peuvent être aggravées.
- Infections fongiques — Des infections fongiques de la cornée peuvent survenir et doivent être envisagées en cas d'ulcération cornéenne persistante.
- Vision trouble — La vision peut être temporairement trouble après l'instillation de TOBRADEX ®ST. Une prudence doit être exercée lors de l'utilisation de machines ou de la conduite d'un véhicule.
- Risque de contamination — Ne touchez pas l'embout du flacon à une surface quelconque, cela pourrait contaminer le contenu.
- Utilisation de lentilles de contact — TOBRADEX ®ST contient du chlorure de benzalkonium, un conservateur antimicrobien, qui peut être absorbé par les lentilles de contact souples. Les lentilles de contact ne doivent pas être portées pendant l'utilisation de TOBRADEX®ST.
EFFETS INDÉSIRABLES :
- Les réactions indésirables les plus fréquentes (<4 %) à la tobramycine ophtalmique topique sont l'hypersensibilité et la toxicité oculaire locale, notamment la douleur oculaire, le prurit des paupières, l'œdème palpébral et l'hyperémie conjonctivale.
- Les réactions dues au composant stéroïdien sont une augmentation de la PIO avec un risque possible d'atteinte du nerf optique et de développement d'un glaucome, une cataracte sous-capsulaire et un retard de cicatrisation.
- Le développement d'une infection secondaire a été observé. Des infections fongiques de la cornée peuvent survenir. Une infection bactérienne secondaire de l'œil après suppression des défenses de l'hôte se produit également.
- Les effets indésirables non oculaires (0,5 % à 1 %) comprenaient céphalées et augmentation de la pression artérielle.
Les effets indésirables supplémentaires suivants ont été rapportés avec les composants individuels ci-dessous :
- Aminosides : Neurotoxicité, ototoxicité et néphrotoxicité ont été observées chez des patients recevant une thérapie systémique par aminosides. Les aminosides peuvent aggraver la faiblesse musculaire chez les patients atteints de troubles neuromusculaires connus ou suspectés, tels que la myasthénie grave ou la maladie de Parkinson, en raison de leur effet potentiel sur la fonction neuromusculaire.
- Dexaméthasone : Syndrome de Cushing et suppression surrénalienne peuvent survenir après utilisation de dexaméthasone au-delà des instructions posologiques recommandées chez des patients prédisposés, y compris les enfants et les patients traités par inhibiteurs du CYP3A4.
Veuillez consulter la notice complète pour la prescription.
À propos de MAXITROL
INDICATIONS ET UTILISATIONS :
- Pour les affections inflammatoires oculaires répondant aux corticostéroïdes pour lesquelles un corticostéroïde est indiqué et où une infection bactérienne ou un risque d'infection bactérienne oculaire existe.
- Les corticostéroïdes oculaires sont indiqués dans les affections inflammatoires de la conjonctive palpébrale et bulbaire, de la cornée et du segment antérieur du globe où le risque inhérent à l'utilisation de stéroïdes dans certaines conjonctivites infectieuses est accepté pour obtenir une diminution de l'œdème et de l'inflammation. Ils sont également indiqués dans les uvéites antérieures chroniques et les lésions cornéennes causées par des brûlures chimiques, radiologiques ou thermiques, ou la pénétration de corps étrangers.
- L'utilisation d'un médicament combiné avec un composant anti-infectieux est indiquée lorsque le risque d'infection est élevé ou lorsque l'on s'attend à ce qu'un nombre potentiellement dangereux de bactéries soit présent dans l'œil.
- L'agent anti-infectieux spécifique de ce produit est actif contre les pathogènes oculaires bactériens courants suivants : Staphylococcus aureus, Escherichia coli, Haemophilus influenzae, espèces Klebsiella/Enterobacter, espèces Neisseria, et Pseudomonas aeruginosa.
- Ce produit ne couvre pas de façon adéquate : Serratia marcescens et les streptocoques, y compris Streptococcus pneumoniae.
CONTRE-INDICATIONS :
Maxitrol est contre-indiqué chez les patients atteints de kératite herpétique épithéliale (kératite dendritique), de vaccine, de varicelle, et de nombreuses autres infections virales de la cornée et de la conjonctive, d'infections mycobactériennes de l'œil, de maladies fongiques des structures oculaires, ainsi qu'en cas d'hypersensibilité à l'un des composants du médicament.
AVERTISSEMENTS :
- Maxitrol ne doit pas être injecté ni administré par voie intraoculaire.
- L'utilisation de corticostéroïdes oculaires peut prolonger l'évolution et aggraver la gravité de nombreuses infections virales de l'œil. Une utilisation prolongée peut entraîner un glaucome, avec atteinte du nerf optique, des défauts de l'acuité visuelle et du champ visuel, ainsi que la formation de cataracte sous-capsulaire postérieure. L'utilisation prolongée peut supprimer la réponse de l'hôte et augmenter ainsi le risque d'infection oculaire secondaire.
- Si ce produit est utilisé pendant 10 jours ou plus, la pression intraoculaire doit être surveillée régulièrement.
- Le sulfate de néomycine peut provoquer une sensibilisation cutanée. Une sensibilité aux aminosides administrés localement, tels que la néomycine, peut se produire chez certains patients. Si une hypersensibilité se développe, le traitement doit être interrompu. Une hypersensibilité croisée à d'autres aminosides peut se produire, et la possibilité que les patients sensibilisés à la néomycine topique soient également sensibles à d'autres aminosides topiques et/ou systémiques doit être prise en compte.
PRÉCAUTIONS :
Si l'inflammation ou la douleur persiste plus de 48 heures ou s'aggrave, le patient doit arrêter l'utilisation et consulter un médecin. Il convient d'informer les patients que leur vision peut être temporairement trouble après l'administration de Maxitrol.
EFFETS INDÉSIRABLES :
Les réactions les plus fréquentes liées à la présence de l'ingrédient anti-infectieux sont des sensibilisations allergiques. Les réactions dues au composant stéroïdien sont : élévation de la pression intraoculaire (PIO) avec possible développement d'un glaucome, et atteinte rare du nerf optique ; formation de cataracte sous-capsulaire postérieure ; et retard de cicatrisation des plaies.
Pour consulter la notice complète de Maxitrol, veuillez visiter Maxitrol Prescribing Information.
À propos de Harrow
Harrow, Inc. (Nasdaq : HROW) est un fournisseur de premier plan de solutions de gestion des maladies ophtalmiques en Amérique du Nord, offrant un portefeuille complet de produits qui traitent des affections touchant à la fois l'avant et l'arrière de l'œil, telles que la sécheresse oculaire, la dégénérescence maculaire liée à l'âge humide (ou néovasculaire), la cataracte, les erreurs de réfraction, le glaucome et diverses autres affections de la surface oculaire et maladies de la rétine. Harrow a été fondée avec l'engagement de fournir des médicaments sûrs, efficaces, accessibles et abordables afin d'améliorer l'observance des patients et les résultats cliniques. Pour plus d'informations sur Harrow, veuillez visiter Harrow et nous retrouver sur LinkedIn.
Déclarations prospectives
Avertissement : le contenu de cet article reflète uniquement le point de vue de l'auteur et ne représente en aucun cas la plateforme. Cet article n'est pas destiné à servir de référence pour prendre des décisions d'investissement.
Vous pourriez également aimer
EUR/USD : Le support tient tandis que le choc pétrolier réévalue les taux – ING
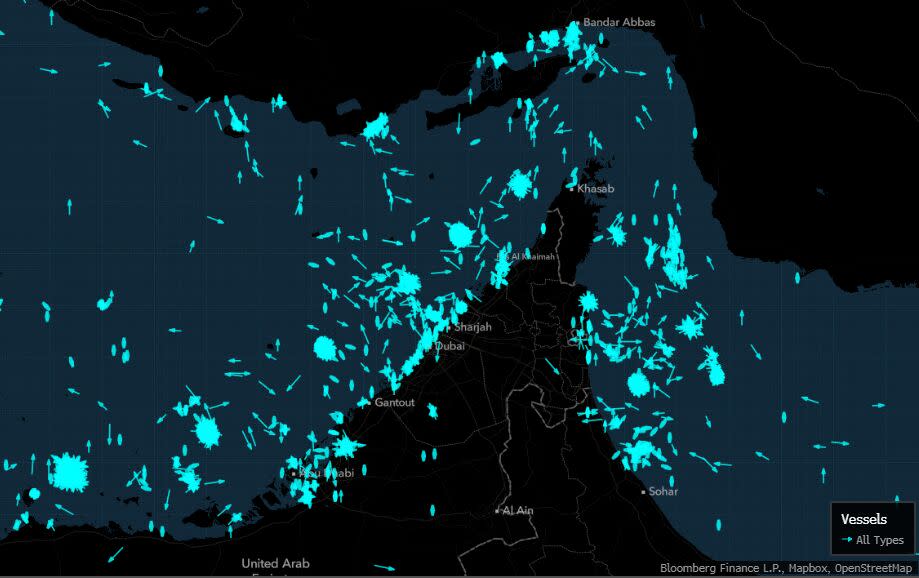
Groupements de navires et tankers rapides suggèrent une activité de brouillage près du détroit d'Hormuz
Egrag Crypto aux traders de XRP : écoutez ce graphique, il nous dit quelque chose